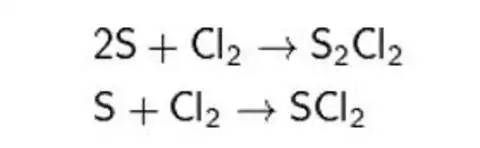Сера (Sulfur) - это
вещество, достаточно широко встречающееся в природе в свободном и связанном состоянии в виде различных минералов и химических соединений, минералы содержащие серу имеют насыщенный желтый цвет различных оттенков
Информация о химическом веществе сера, физические и химические свойства серы и ее соединений, происхождение серы и месторождения серы, место серы в природе и значение серы для живых организмов, добыча серы и производство серы, товарные виды серы и методы производства серы, применение серы в человеческой деятельности, в том числе применение серы в химической промышленности, применение серы в бумажной промышленности, применение серы в медицине, вред серы для окружающей среды, мировой рынок серы, в том числе мировая добыча серы и мировое производство серы, мировые цены на серу
Структура публикации
- Сера - это, определение
- Этимология слова «сера»
- Происхождение серы
- Природные минералы серы
- Месторождения серы
- Сера в живых организмах
- Роль серы в организме человека
- Свойства серы
- Физические свойства серы
- Твердое состояние серы
- Жидкое состояние серы
- Газообразное состояние серы
- Химические свойства серы
- История открытия серы
- Получение серы
- Получение серы методом подземной выплавки
- Получение серы из серных руд на заводах
- Термический метод получения серы
- Пароводяной метод получения серы
- Экстракционный метод получения серы
- Комбинированный метод получения серы
- Центрифугальный метод извлечения серы
- Получение серы из природного газа
- Товарные формы серы
- Комовая сера
- Жидкая сера
- Формованная сера
- Гранулированная сера
- Молотая сера
- Коллоидная сера
- Высокочистая сера
- Применение серы
- Сера в производстве серной кислоты
- Сера в производстве спичек
- Сера в производстве смазочных веществ
- Сера в производстве взрывчатых веществ
- Сера в производстве целлюлозы
- Сера в вулканизации каучуков
- Сера в строительстве
- Сера в сельском хозяйстве
- Сера в медицине и фармацевтике
- Сера в косметике
- Вред серы для окружающей среды
- Химическое отравление природы
- Пожароопасность серы
- Пожары на складах серы
- Мировой рынок серы
- Мировая добыча серы
- Мировое производство серы
- Крупнейшие мировые производители серы
- Мировое потребление серы
- Мировые цены на серу
- Авторы, источники и ссылки
- Создатель статьи
- Ответственные администраторы
- Источники текстов
- Использованные сервисы
Сера - это, определение
Сера - это элемент периодической таблицы химических элементов Менделеева, имеющий атомное число 16. В природе сера встречается в виде самородков и в связанном виде в качестве химических соединений. Свойства серы известны с древних времен, человечество занимается добычей и производством серы несколько тысяч лет, применяя полученное вещество в различных областях жизнедеятельности, таких как медицина, производство пороха и ритуальные обряды.
Сера - это элемент 16-й группы (по устаревшей классификации - главной подгруппы VI группы), третьего периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, с атомным номером 16. Проявляет неметаллические свойства. Обозначается символом S (лат. sulfur). В водородных и кислородных соединениях находится в составе различных ионов, образует многие кислоты и соли. Многие серосодержащие соли малорастворимы в воде.
Сера - это S (sulfur), неметаллический химический элемент, член семейства халькогенов (O, S, Se, Te и Po) - IVA подгруппы периодической системы элементов.
Сера - это одно из простых (несложных, неразлагаемых) веществ, плавкое и сильно горючее ископаемое вулканического рожденья; как товар, зовут ее: сера горючая.
Сера - это химический элемент VI группы периодической системы; атомный номер 16, атомная масса 32,066; относится к халькогенам; неметалл желтого цвета; tпл 110,2шC (a S) и 115,21шC (b S).
Сера - это твердое вещество желтого цвета; в природе встречается как в свободном виде, так и в виде различных соединений.
Сера - это металлоид, легко воспламеняющееся вещество желтоватого или сероватого цвета, применяемое в медицине и технике.
Сера - это минерал лимонно-желтого цвета, иногда медово-жёлтого, желтовато-серого или коричневатого, представляет собой молекулярную серу - S, минерал очень хрупкий, твердость 1-2.
Сера - это химический элемент, легко воспламеняющееся вещество желтого или сероватого цвета.
Этимология слова «сера»
Слово «сера», известное в древнерусском языке с XV в., заимствовано из старославянского «сѣра» - «сера, смола», вообще «горючее вещество, жир». Этимология слова не выяснена до настоящих времен, поскольку первоначальное общеславянское название вещества утрачено и слово дошло до современного русского языка в искаженном виде.
По предположению Фасмера, «сера» восходит к лат. сera - «воск» или лат. serum - «сыворотка».
Латинское sulfur (происходящее из эллинизированного написания этимологического sulpur) предположительно восходит к индоевропейскому корню swelp - «гореть».
Происхождение серы
Большие скопления самородной серы встречаются не так уж часто. Чаще она присутствует в некоторых рудах. Руда самородной серы - это порода с вкраплениями чистой серы.
От того, образовались эти вкрапления одновременно с сопутствующими породами или позже, зависит направление поисковых и разведочных работ. Существует несколько совершенно различных теорий по этому вопросу.
Теория сингенеза (то есть одновременного образования серы и вмещающих пород) предполагает, что образование самородной серы происходило в мелководных бассейнах. Особые бактерии восстанавливали сульфаты, растворённые в воде, до сероводорода, который поднимался вверх, попадал в окислительную зону и здесь химическим путём или при участии других бактерий окислялся до элементарной серы. Сера осаждалась на дно, и впоследствии содержащий серу ил образовал руду.
Теория эпигенеза (вкрапления серы образовались позднее, чем основные породы) имеет несколько вариантов. Самый распространённый из них предполагает, что подземные воды, проникая сквозь толщи пород, обогащаются сульфатами.
Если такие воды соприкасаются с месторождениями нефти или Природного газа, то ионы сульфатов восстанавливаются углеводородами до сероводорода. Сероводород поднимается к поверхности и, окисляясь, выделяет чистую серу в пустотах и трещинах пород.
В последние десятилетия находит всё новые подтверждения одна из разновидностей теории эпигенеза - теория метасоматоза (в переводе с греческого «метасоматоз» означает замещение). Согласно ей в недрах постоянно происходит превращение гипса CaSO4-H2O и ангидрита CaSO4 в серу и кальцит СаСО3. Эта теория создана в 1935 году советскими учёными Л. М. Миропольским и Б. П. Кротовым. В её пользу говорит, в частности, такой факт.
В 1961 году в Ираке было открыто месторождение Мишрак. Сера здесь заключена в карбонатных породах, которые образуют свод, поддерживаемый уходящими вглубь опорами (в геологии их называют крыльями). Крылья эти состоят в основном из ангидрита и гипса. Такая же картина наблюдалась на отечественном месторождении Шор-Су.
Геологическое своеобразие этих месторождений можно объяснить только с позиций теории метасоматоза: первичные гипсы и ангидриты превратились во вторичные карбонатные руды с вкраплениями самородной серы.
Важно не только соседство минералов - среднее содержание серы в руде этих месторождений равно содержанию химически связанной серы в ангидрите. А исследования изотопного состава серы и углерода в руде этих месторождений дали сторонникам теории метасоматоза дополнительные аргументы.
Но есть одно «но»: химизм процесса превращения гипса в серу и кальцит пока не ясен, и потому нет оснований считать теорию метасоматоза единственно правильной. На земле и сейчас существуют озёра (в частности, Серное озеро близ Серноводска), где происходит сингенетическое отложение серы и сероносный ил не содержит ни гипса, ни ангидрита.
Всё это означает, что разнообразие теорий и гипотез о происхождении самородной серы - результат не только и не столько неполноты наших знаний, сколько сложности явлений, происходящих в недрах. Ещё из элементарной школьной математики все мы знаем, что к одному результату могут привести разные пути. Этот закон распространяется и на геохимию.
Природные минералы серы
Сера является шестнадцатым по химической распространённости элементом в земной коре. Встречается в свободном (самородном) состоянии и связанном виде.
Сера относится к весьма распространенным химическим элементам (кларк 4,7·10-2); встречается в свободном состоянии (самородная сера) и в виде соединений - сульфидов, полисульфидов, сульфатов.
Вода морей и океанов содержит сульфаты натрия, магния, кальция. Известно более 200 минералов серы, образующихся при эндогенных процессах.
В биосфере образуется свыше 150 минералов серы (преимущественно сульфатов); широко распространены процессы окисления сульфидов до сульфатов, которые в свою очередь восстанавливаются до вторичного H2S и сульфидов. Эти реакции происходят при участии микроорганизмов.
Многие процессы биосферы приводят к концентрации серы - она накапливается в гумусе почв, углях, нефти, морях и океанах (8,9·10-2%), подземных водах, в озерах и солончаках. В глинах и сланцах серы в 6 раз больше, чем в земной коре в целом, в гипсе - в 200 раз, в подземных сульфатных водах - в десятки раз.
В биосфере происходит круговорот серы: она приносится на материки с атмосферными осадками и возвращается в океан со стоком. Источником серы в геологическом прошлом Земли служили главным образом продукты извержения вулканов, содержащие SO2 и H2S. Хозяйственная деятельность человека ускорила миграцию серы; интенсифицировалось окисление сульфидов.
Важнейшие природные минералы серы:
- FeS2 - железный колчедан или пирит;
- ZnS - цинковая обманка или сфалерит (вюрцит);
- PbS - свинцовый блеск или галенит;
- HgS - киноварь;
- Sb2S3 - антимонит.
Кроме того, сера присутствует в нефти, природном угле, природных газах и сланцах. Сера - шестой элемент по содержанию в природных водах, встречается в основном в виде сульфат-иона и обусловливает «постоянную» жёсткость пресной воды. Жизненно важный элемент для высших организмов, составная часть многих белков, концентрируется в волосах.
Месторождения серы
Сера участвует в разнообразных геолого-геохимических процессах, многие из которых приводят к её выделению в самородном виде, однако лишь некоторые из них ведут к накоплению серы в виде промышленных месторождений.
Главным является инфильтрационно-метасоматический тип серных руд (более 90% мировых запасов). Образование их происходит там, где сульфатные или карбонатно-сульфатные породы благодаря структурно-тектоническим условиям оказываются на пути инфильтрации с глубины углеводородов, вступающих во взаимодействие с этими породами и метасоматически преобразующих их в серные руды.
Месторождения этого типа развиты среди нормально-осадочных толщ и в кепроках соляных куполов. Инфильтрационно-метасоматические месторождения приурочены к карбонатно-сульфатным комплексам галогенных формаций, к зонам сочленения поднятий и прогибов, к антиклинальным, купольным и другим положительным структурам в связи с разрывными нарушениями, зонами дробления, трещиноватости; они пространственно и генетически связаны с углеводородами.
Распространённым генетическим типом является самородная сера, образующаяся при окислении сероводорода, растворённого в подземных водах или выделяющегося в виде газовых струй. Попадая в окислительные условия сероводород образует плёнки, примазки, прожилки и другие выделения серы, которые не создают значительных накоплений, отвечающих современным требованиям промышленности, хотя раньше этот тип серных руд широко эксплуатировался.
Накопления вулканогенной серы весьма разнообразны: выделение самородной серы в приповерхностной зоне в виде крустификаций, импрегнаций, выполнений. Они широко распространены, но не образуют больших скоплений.
Более существенное значение имеют гидротермально-метасоматические вулканогенные месторождения, на которых развиты серные кварциты и опалиты, серно-алунитовые кварциты и другие типы серных руд, образующихся в результате гидротермального воздействия вулканических сернистых газов и растворов на эффузивные породы, туфы, туфобрекчии, а также вулканогенно-осадочные накопления серы в кратерных озёрах.
Месторождения серных руд (карта) концентрируются в Мексиканского залива сероносной провинции, Средиземноморской сероносной провинции, включающей Предкарпатский сероносный бассейн, Среднеазиатской сероносной провинции, Восточно-Европейской сероносной провинции, Кордильерской провинции, охватывающей территории Чили, Перу, Боливии, Колумбии, Коста-Рики и США, и в Восточно-Азиатской провинции, протягивающейся от полуострова Камчатка до Новой Зеландии.
Залежи серы широко распространены на территории Средней Азии, месторождения Гаурдак, Шор-Су - в трещинах и пустотах различных осадочных пород в ассоциации с нефтью, гипсом, целестином, кальцитом, арагонитом и др.
В Кара-Кумской пустыне в виде бугров, прикрытых кремнистыми корками, в ассоциации с гипсом, кварцем, халцедоном, опалом и др.
Большие осадочные месторождения имеются в Поволжье (в районе города Куйбышева).
Большой известностью пользуются месторождения Сицилии, мощные месторождения в штатах Техас и Луизиана (США), Боливии, Мишрак и Ираке, Южная Польша, Штасфурт в Германии.
В природе сера встречается как россыпями, так и в виде кристаллических пластов, иногда образуя изумительные по красоте группы полупрозрачных желтых кристаллов (так называемые друзы).
В вулканических местностях часто наблюдается выделение из-под земли газа сероводорода H2S; в этих же регионах сероводород встречается в растворенном виде в серных водах. Вулканические газы часто содержат также сернистый газ SO2.
Области вулканизма: Камчатка, Япония, Италия, Индонезия.
Сера в живых организмах
В виде органических и неорганических соединений сера постоянно присутствует во всех живых организмах и является важным биогенным элементом. Ее среднее содержание в расчете на сухое вещество составляет: в морских растениях около 1,2%, наземных - 0,3%, в морских животных 0,5-2%, наземных - 0,5%.
Биологическая роль серы определяется тем, что она входит в состав широко распространенных в живой природе соединений:
- аминокислот (метионин, цистеин), и следовательно белков и пептидов;
- коферментов (кофермент А, липоевая кислота), витаминов (биотин, тиамин), глутатиона и других.
Сульфгидрилъные группы (-SH) остатков цистеина играют важную роль в структуре и каталитической активности многих ферментов. Образуя дисульфидные связи (-S-S-) внутри отдельных полипептидных цепей и между ними, эти группы участвуют в поддержании пространственной структуры молекул белков.
У животных сера обнаружена также в виде органических сульфатов и сульфокислот - хондроитинсерной кислоты (в хрящах и костях), таурохолиевой кислоты (в желчи), гепарина, таурина. В некоторых железосодержащих белках (например, ферродоксинах) сера обнаружена в форме кислотолабильного сульфида. Сера способна к образованию богатых энергией связей в макроэргических соединениях.
Неорганические соединения серы в организмах высших животных обнаружены в небольших количествах, главным образом в виде сульфатов (в крови, моче), а также роданидов (в слюне, желудочном соке, молоке, моче).
Морские организмы богаче неорганическими соединениями серы, чем пресноводные и наземные. Для растений и многих микроорганизмов сульфат (SO42-) наряду с фосфатом и нитратом служит важнейшим источником минерального питания.
Перед включением в органические соединения сера претерпевает изменения в валентности и превращается затем в органических форму в своем наименее окисленном состоянии; таким образом сера широко участвует в окислительно-восстановительных реакциях в клетках.
В клетках сульфаты, взаимодействуя с аденозинтрифосфатом (АТФ), превращаются в активную форму - аденилилсульфат.
Катализирующий эту реакцию фермент - сульфурилаза (АТФ:сульфат -аденилилтрансфераза) широко распространен в природе. В такой активированной форме сульфонильная группа подвергается дальнейшим превращениям - переносится на другой акцептор или восстанавливается.
Животные усваивают серу в составе органических соединений. Автотрофные организмы получают всю серу, содержащуюся в клетках, из неорганических соединений, главным образом в виде сульфатов. Способностью к автотрофному усвоению серы обладают высшие растения, многие водоросли, грибы и бактерии. (Из культуры бактерий был выделен специальный белок, осуществляющий перенос сульфата через клеточную мембрану из среды в клетку.)
Большую роль в круговороте серы в природе играют микроорганизмы - десульфурирующие бактерии и серобактерии. Многие разрабатываемые месторождения серы - биогенного происхождения. Сера входит в состав антибиотиков (пенициллины, цефалоспорины); ее соединения используются в качестве радиозащитных средств, средств защиты растений.
Роль серы в организме человека
Сера является одним из наиболее распространенных минералов в организме человека. Сера является структурной частью большинство белков и, таким образом принимает участие в активности фермента, антигена, и много различных тканей. Сера- это минерал, который имеет важное значение для всех живых существ: аминокислоты, цистеин, метионин, все содержат серу, и поэтому все полипептиды, белки и ферменты, которые содержат эти аминокислот, также содержат и серу.
Источники серы в продуктах питания - серу можно найти в яйцах, бразильских орехах, бобовых, чесноке, луке, капусте, горчице, спарже, зародышах пшеницы, хрене, брюссельском капусте, цветной капусте, трюфели, кресс-салате, луке-порей, редиске и т.д. Недостаток серы приводит к дегенерации коллагена, хрящей, связок и сухожилий. Сера помогает при артрите.
Недавние исследования показали, что этот минерал имеет очень важное значение. Многие, наверное, не потребляют достаточное количество серы. Около половина количества серы в нашем организме можно найти в мышцах, коже и костях, в то время как остальное служит для других частей тела.
Сера играет важную роль в различных системах организма, он помогает в формировании белков и их связей. Волосы и ногти состоят в основном из белка, называемого кератином, белок, который содержит большое количество серы.
Связки и сухожилия состоят из белка, которые содержат серы, что дает им их гибкость. Когда человек становится старым , сухожилия и связки теряют свою гибкость и поэтому есть больше проблем с кожей, твердые мышцы и боли в суставах. Недостаток сера способствует эти проблемы, связанные со старением.
Сера помогает надлежащей активности инсулина и ликвидации яда в организме.
Дополняет белки, сера необходима структуре и активности ферментов. Если нет серы, ферменты не могут работать правильно, и что может вызвать различные проблемы со здоровьем. Это потому, что если есть неправильные ферменты метаболизма процессы не могут работать должным образом.
Правильное содержание серы поддерживает метаболический баланс и повышает производительность механизмов коагуляции. Сера является частью витаминов В. Сера считается важным материалом в формировании кожи. Сера также строительный материал для хрящей и соединительной ткани, и поэтому она имеет важное значение для лечения ран и травм.
С древних времен купание в природных источниках с высокой концентрацией серы считалось целебными источниками. Во всем мире, Спа центры были построены вокруг источников, которые содержат серную воду.
Некоторые относят чеснок к медицинским преимуществам, потому что у чеснока высокий уровень серы. Лечебное использование чеснока существовало в культурах с древних времен. Хотя продукты Западных культур содержат большое количество белка, но не всегда содержат достаточное количество серы, так как использование серы в качестве подкормки растений снизилась.
Свойства серы
Сера имеет вид желтого порошка или хрупкой кристаллической массы без запаха и вкуса и нерастворима в воде.
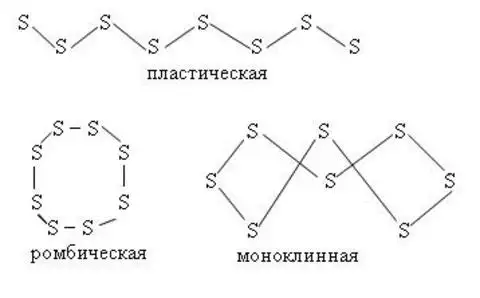
Для серы характерны несколько аллотропных модификаций. Наиболее известны следующие:
- кристаллическая сера - ромбическая (самородная сера, a-S) и моноклинная (призматическая сера, b-S);
- аморфная - коллоидная (серное молоко) и пластическая;
- промежуточная аморфно-кристаллическая - сублимированная (серный цвет).
Физические свойства серы
Сера существенно отличается от кислорода способностью образовывать устойчивые цепочки и циклы из атомов.
Твердое состояние серы
Наиболее стабильны циклические молекулы S8, имеющие форму короны, образующие ромбическую и моноклинную серу. Это кристаллическая сера - хрупкое вещество жёлтого цвета.
Кристаллическая сера имеет две модификации; одну из них, ромбическую, получают из раствора серы в сероуглероде (CS2) испарением растворителя при комнатной температуре. При этом образуются ромбовидные просвечивающие кристаллы светложелтого цвета, легко растворимые в CS2. Эта модификация устойчива до 96° С, при более высокой температуре стабильна моноклинная форма.
При естественном охлаждении расплавленной серы в цилиндрических тиглях вырастают крупные кристаллы ромбической модификации с искаженной формой (октаэдры, у которых частично «срезаны» углы или грани). Такой материал в промышленности называется комовая сера.
Моноклинная модификация серы представляет собой длинные прозрачные темножелтые игольчатые кристаллы, также растворимые в CS2. При охлаждении моноклинной серы ниже 96° С образуется более стабильная желтая ромбическая сера.
Твердая сера существует также в двух некристаллических, аморфных, формах. Коллоидная сера получается при осаждении серы из раствора (например, при кипячении серы с известью) и фильтровании с последующим добавлением хлороводородной кислоты к прозрачному фильтрату.
Осадок представляет собой мелкодисперсную белую и хорошо растворимую в CS2 серу. Коллоидную серу используют в медицине как антисептик, слабительное и противопаразитическое средство в виде порошков и мазей.
Другая некристаллическая форма - пластическая сера - образуется при резком охлаждении расплава, например, холодной водой. Пластическая сера бывает темнокрасного или коричневого цвета, она каучукоподобна (плотность 2,046 г/см3) и не растворяется в CS2; при хранении становится хрупкой, желтеет и по мере превращения в ромбическую все лучше растворяется в CS2.
В дополнение к этим кристаллическим и аморфным формам существует промежуточная форма, известная как серный цвет или сублимированная сера, которая получается конденсацией паров серы, минуя жидкую фазу.
Она состоит из мельчайших зерен, имеющих центр кристаллизации и аморфную поверхность. Эта форма медленно и не полностью растворяется в CS2. После обработки аммиаком для очистки от таких примесей, как мышьяк, получается продукт, известный в медицине как промытая сера, которая используется аналогично коллоидной сере.
Формулу серы чаще всего записывают просто S, так как она, хотя и имеет молекулярную структуру, является смесью простых веществ с разными молекулами. В воде сера нерастворима, но хорошо растворяется в органических растворителях, например, в сероуглероде, скипидаре.
Жидкое состояние серы
Молекулы серы состоят из замкнутой цепочки восьми атомов (S8). Жидкая сера обладает необычным свойством: с повышением температуры ее вязкость увеличивается. Ниже 160° С сера - типичная жидкость желтоватого цвета, ее состав соответствует формуле S8 и обозначается l-S. Плавление серы сопровождается заметным увеличением объёма (примерно 15 %).
С повышением температуры кольцевые молекулы S8 начинают разрываться и соединяться друг с другом, образуя длинные цепи (m-S), цвет жидкой серы становится темнокрасным, вязкость возрастает, достигая максимума при 200–250° С.
Наибольшую вязкость расплав серы приобретает при температуре 190 °C; дальнейшее повышение температуры сопровождается уменьшением вязкости и выше 300 °C расплавленная сера снова становится подвижной. Это связано с тем, что при нагревании серы она постепенно полимеризуется, увеличивая длину цепочки с повышением температуры. При нагревании серы свыше 190 °C полимерные звенья начинают рушиться.
Газообразное состояние серы
Сера кипит при 444,6° C, образуя оранжево-желтые пары, состоящие преимущественно из молекул S8. С повышением температуры окраска паров переходит в темнокрасную, затем в палевую, а при 650° C в соломенно-желтую.
При дальнейшем нагревании молекулы S8 диссоциируют, образуя равновесные формы S6, S4 и S2 при разных температурах. И, наконец, при >1000° С пары состоят практически из молекул S2, а при 2000° С - из одноатомных молекул.
Сера может служить простейшим примером электрета. При трении сера приобретает сильный отрицательный заряд.
Химические свойства серы
Сера - типичный неметалл. На внешней электронной оболочке у нее шесть электронов, и она легче присоединяет электроны других элементов, чем отдает свои. Со многими металлами реагирует с выделением тепла (например, при соединении с медью, железом, цинком). Она соединяется и почти со всеми неметаллами, хотя не так энергично.
На воздухе сера горит, образуя сернистый ангидрид - бесцветный газ с резким запахом:
С помощью спектрального анализа установлено, что на самом деле процесс окисления серы в двуокись представляет собой цепную реакцию и происходит с образованием ряда промежуточных продуктов:
- моноокиси серы S2O2;
- молекулярной серы S2;
- свободных атомов серы S;
- свободных радикалов моноокиси серы SO.
Восстановительные свойства серы проявляются в реакциях серы и с другими неметаллами, однако при комнатной температуре сера реагирует только со фтором:
Расплав серы реагирует с хлором, при этом возможно образование двух низших хлоридов (дихлорид серы и дитиодихлорид):
При избытке серы также образуются разнообразные дихлориды полисеры типа SnCl2.
При нагревании сера также реагирует с фосфором, образуя смесь сульфидов фосфора, среди которых - высший сульфид P2S5:
Кроме того, при нагревании сера реагирует с водородом, углеродом, кремнием:
При нагревании сера взаимодействует со многими металлами, часто - весьма бурно. Иногда смесь металла с серой загорается при поджигании. При этом взаимодействии образуются сульфиды:
Растворы сульфидов щелочных металлов реагируют с серой с образованием полисульфидов:
Из сложных веществ следует отметить прежде всего реакцию серы с расплавленной щёлочью, в которой сера диспропорционирует аналогично хлору:
Полученный сплав называется серной печенью.
С концентрированными кислотами-окислителями (HNO3, H2SO4) сера реагирует только при длительном нагревании:
При увеличении температуры в парах серы происходят изменения в количественном молекулярном составе. Число атомов в молекуле уменьшается:
При 800-1400 °C пары состоят в основном из двухатомной серы:
А при 1700 °C сера становится атомарной:
История открытия серы
Сера в самородном состоянии, а также в виде сернистых соединений известна с древнейших времён.
Сера встречается в природе в свободном (самородном) состоянии, поэтому она была известна человеку уже в глубокой древности. Сера привлекала внимание характерной окраской, голубым цветом пламени и специфическим запахом, возникающим при горении (запах сернистого газа).
С запахом горящей серы, удушающим действием сернистого газа и отвратительным запахом сероводорода человек познакомился, вероятно, ещё в доисторические времена.
Именно из-за этих свойств сера использовалась жрецами в составе священных курений при религиозных обрядах. Сера считалась произведением сверхчеловеческих существ из мира духов или подземных богов.
Считалось, что горящая сера отгоняет нечистую силу. В Библии говорится об использовании серы для очищения грешников. У человека средневековья запах «серы» ассоциировался с преисподней. Применение горящей серы для дезинфекции упоминается Гомером. В Древнем Риме с помощью сернистого газа отбеливали ткани.
Очень давно сера стала применяться в составе различных горючих смесей для военных целей. Уже у Гомера описаны «сернистые испарения», смертельное действие выделений горящей серы. Сера, вероятно, входила в состав «греческого огня», наводившего ужас на противников.
Около VIII в. китайцы стали использовать её в пиротехнических смесях, в частности, в смеси типа пороха. Горючесть серы, лёгкость, с которой она соединяется с металлами с образованием сульфидов (например, на поверхности кусков металла), объясняют то, что её считали «принципом горючести» и обязательной составной частью металлических руд.
Пресвитер Теофил (XII в.) описывает способ окислительного обжига сульфидной медной руды, известный, вероятно, ещё в древнем Египте.
В период арабской алхимии возникла ртутно-серная теория состава металлов, согласно которой сера почиталась обязательной составной частью (отцом) всех металлов. В дальнейшем она стала одним из трёх принципов алхимиков, а позднее «принцип горючести» явился основой теории флогистона.
Элементарную природу серы установил Лавуазье в своих опытах по сжиганию. С введением пороха в Европе началось развитие добычи природной серы, а также разработка способа получения её из пиритов; последний был распространён в древней Руси. Впервые в литературе он описан у Агриколы.
Таким образом, точно происхождение серы не установлено, но, как сказано выше, этот элемент использовался до Рождества Христова, а значит, знаком людям с давних времён.
Получение серы
В древности и в средние века серу добывали, вкапывая в землю большой глиняный горшок, на который ставили другой, с отверстием в дне. Последний заполняли породой, содержащей серу, и затем нагревали. Сера плавилась и стекала в нижний горшок.
В настоящее время серу получают главным образом путём выплавки самородной серы непосредственно в местах её залегания под землёй. Серные руды добывают разными способами - в зависимости от условий залегания. Залежам серы почти всегда сопутствуют скопления ядовитых газов - соединений серы. К тому же нельзя забывать о возможности её самовозгорания.
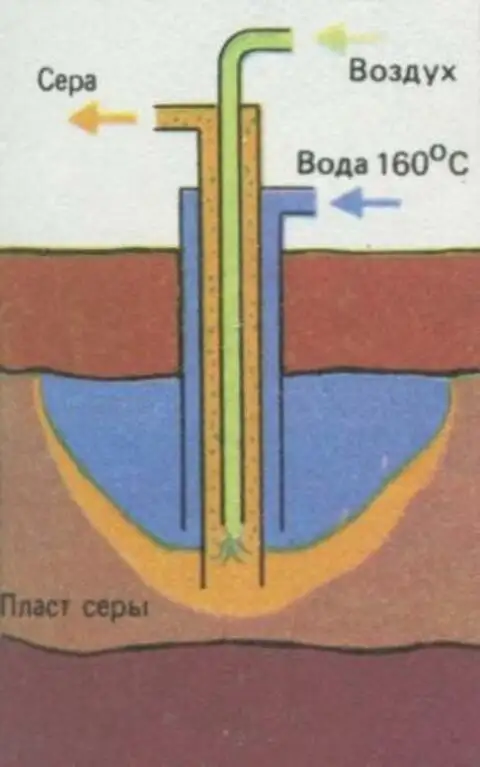
Получение серы методом подземной выплавки
В конце прошлого века на юге Соединенных Штатов были открыты богатейшие месторождения серной руды. Но подступиться к пластам было непросто: в шахты (а именно шахтным способом предполагалось разрабатывать месторождение) просачивался сероводород и преграждал доступ к сере. Кроме того, пробиться к сероносным пластам мешали песчаные плавуны.
Выход нашел химик Герман Фраш, предложивший плавить серу под землей и через скважины, подобные нефтяным, выкачивать ее на поверхность. Сравнительно невысокая (меньше 120°C) температура плавления серы подтверждала реальность идеи Фраша. В 1890 г. начались испытания, приведшие к успеху.
В принципе установка Фраша очень несложна: труба в трубе. В пространство между трубами подается перегретая вода и по нему идет в пласт. А по внутренней, обогреваемой со всех сторон, трубе поднимается расплавленная сера.
Современный вариант установки Фраша дополнен третьей - самой узкой трубой. Через нее в скважину подается сжатый воздух, который помогает поднять расплавленную Серу на поверхность. Одно из основных достоинств метода Фраша - в том, что он позволяет уже на первой стадии добычи получить сравнительно чистую серу. При разработке богатых руд этот метод весьма эффективен.
Раньше считалось, что метод подземной выплавки серы применим только в специфических условиях «соляных куполов» тихоокеанского побережья США и Мексики. Однако опыты, проведенные в Польше и СССР, опровергли это мнение. В Польше этим методом уже добывают большое количество серы: в 1968 г. пущены первые серные скважины и в СССР.
Получение серы из серных руд на заводах
Руду, полученную в карьерах и шахтах, приходится перерабатывать (часто с предварительным обогащением), используя для этого различные технологические приемы.
При добыче руды открытым способом экскаваторами снимают пласты пород, под которыми залегает руда. Взрывами рудный пласт дробят, после чего глыбы руды отправляют на сероплавильный завод, где из концентрата извлекают серу.
Известно несколько методов получения серы из серных руд - пароводяные, фильтрационные, термические, центрифугальные и экстракционные.
Термический метод получения серы
Термические методы извлечения серы - самые старые. Еще в XVIII в. в Неаполитанском королевстве выплавляли серу в кучах - «сольфатарах». До сих пор в Италии выплавляют серу в примитивных печах - «калькаронах». Тепло, необходимое для выплавления серы из руды, получают, сжигая часть добытой серы. Процесс этот малоэффективен, потери достигают 45%.
По термическому методу серу либо выплавляют из дробленой руды в камерных печах, либо возгоняют во вращающихся печах.
Выплавка серы производится в многокамерных печах (чаще шести камерных), представляющих собой аппарат полу непрерывного действия. Многокамерные печи состоят из нескольких кирпичных цилиндрических камер (шахт) с наклонным подом, соединенных друг с другом газоходами.
Кусковую руду загружают через загрузочную воронку, расположенную в верхней части камеры. Горячий воздух, поступающий в первую камеру, расплавляет серу, которая стекает по наклонному поду в приемник. Некоторая часть серы испаряется и частично сгорает до сернистого газа. Оставшаяся в первой камере пустая порода - огарок подогревает поступающие новые порции воздуха, которые плавят серу в следующей печи.
В последующих камерах происходит подогрев руды и конденсация паров серы, испарившейся в предыдущих камерах. После охлаждения огарка в первой камере его выгружают, в камеру загружают новые порции руды и подключают ее к предпоследней камере (по ходу газа). При такой работе печей происходит максимальное использование тепла огарка и газа.
При выплавке серы в многокамерных печах используют руды, содержащие не менее 18% серы и не рассыпающиеся после ее выплавки. Около 30% серы сгорает до сернистого газа, используемого в производстве серной кислоты. В этом случае выход серы (включая и содержащуюся в сернистом газе) достигает 98%.
Пароводяной метод получения серы
Италия стала родиной и пароводяных методов извлечения серы из руд. В 1859 г. Джузеппе Джилль получил патент на свой аппарат - предшественник нынешних автоклавов. Автоклавный метод (значительно усовершенствованный, конечно) используется и сейчас во многих странах.
Пароводяной метод (для руд с высоким содержанием серы) заключается в обработке дробленой руды в автоклавах острым Паром.
В автоклавном процессе обогащенный концентрат серной руды, содержащий до 80% серы, в виде жидкой пульпы с реагентами подается насосами в автоклав. Туда же под давлением подается водяной пар. Пульпа нагревается до 130°C. Сера, содержащаяся в концентрате, плавится и отделяется от породы. После недолгого отстоя выплавленная сера сливается. Затем из автоклава выпускаются «хвосты» - взвесь пустой породы в воде. Хвосты содержат довольно много серы и вновь поступают на обогатительную фабрику.
Степень извлечения серы из кусковой породы в автоклавах зависит от степени измельчения руды и особенно от количества содержащейся в ней серы. При небольшом ее содержании, например 20%, из кусковой руды выплавляется около половины серы, и поэтому бедные руды перерабатывать в автоклавах невыгодно.
При переработке богатого серой сырья, например концентратов (обогащенной руды), выход доходит до 80% и более. Иногда при выплавке серы в автоклав добавляют керосин, мазут или другие поверхностно-активные вещества, способствующие разделению капель серы и мельчайших частичек пустой породы, всплывающих наверх водного слоя.
В Российской Федерации автоклавный способ был впервые применен инженером К.Г. Паткановым в 1896 г.
Современные автоклавы - это огромные аппараты высотой с четырехэтажный дом. Такие автоклавы установлены, в частности, на сероплавильном заводе Роздольского горно-химического комбината в Прикарпатье.
Экстракционный метод получения серы
Экстракционные методы основаны на извлечении серы из руды растворителями (например, сероуглеродом). Эти методы требуют больших материальных затрат и применяются довольно редко.
Экстракционный метод (применяется ограниченно) состоит в извлечении серы из руд сероуглеродом.
Комбинированный метод получения серы
Комбинированный метод включает флотационное обогащение серной руды и следующее извлечение серы из приобретенного концентрата. Метод обеспечивает высочайшее качество S (99,9 %), но имеет значимый недочет - высочайшее содержание серы в отходах производства (30-40 %).
На некоторых производствах, например на крупном серном комбинате в Тарнобжеге (Польша), пустую породу отделяют от расплавленной серы на специальных фильтрах.
Центрифугальный метод извлечения серы
Также известен способ разделения серы на центрифугах. Только этот способ имеет недостаток: сера получается с примесями. И тогда необходимо проводить ее дополнительную очистку.
Метод разделения серы и пустой породы на центрифугах разработан в нашей стране. Словом, «руду золотую (точнее - золотистую) отделять от породы пустой» можно по-разному.
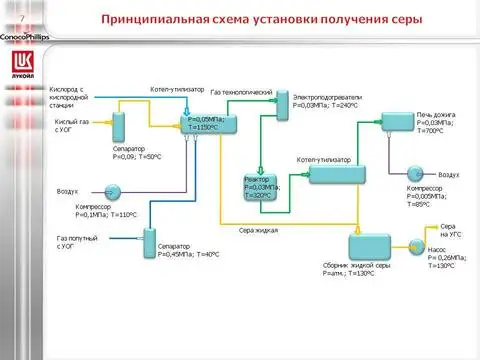
Получение серы из природного газа
Также сера в больших количествах содержится в Природном газе в газообразном состоянии (в виде сероводорода, сернистого ангидрида). При добыче она откладывается на стенках труб и оборудования, выводя их из строя. Поэтому её улавливают из газа как можно быстрее после добычи. Полученная химически чистая мелкодисперсная сера является идеальным сырьём для химической и резиновой промышленности.
Серу из природного сернистого газа получают методом Клауса. Для этого используются так называемые серные ямы, где происходит дегазация серы, на выходе получают модифицированную серу - продукт, широко использующийся в производстве асфальта.
Технологические установки для получения серы обычно включают в себя ямы недегазированной серы, ямы дегазации, ямы хранения дегазированной серы, а также налив жидкой серы и склад комовой серы.
Стены ямы обычно делают из кирпича, дно заливают бетоном, а сверху закрывают яму алюминиевой крышей. Так как сера - это весьма агрессивная среда, ямы периодически приходится полностью реконструировать.
Крупнейшее месторождение самородной серы вулканического происхождения находится на острове Итуруп с запасами категории A+B+C1 - 4227 тыс. тонн и категории C2 - 895 тыс. тонн, что достаточно для строительства предприятия мощностью 200 тыс. тонн гранулированной серы в год.
Товарные формы серы
В промышленности реализовано получение серы в различных товарных формах. Выбор той или иной формы определяется требованиями заказчика.
Комовая сера
Комовая сера до начала 1970-х годов была основным видом серы, выпускаемым промышленностью СССР. Ее получение технологически просто и осуществляется подачей жидкой серы по обогреваемому трубопроводу на склад, где производится заливка серных блоков.
Застывшие блоки высотой 1-3 метра разрушают на более мелкие куски и транспортируют заказчику. Метод, однако, имеет недостатки: невысокое качество серы, потери на пыль и крошку при рыхлении и погрузке, сложность автоматизации.
Жидкая сера
Жидкую серу хранят в обогреваемых резервуарах и транспортируют в цистернах. Транспорт жидкой серы более выгоден, чем ее плавление на месте. Достоинства получения жидкой серы - отсутствие потерь и высокая чистота. Недостатки - опасность возгорания, траты на обогрев цистерн.
Формованная сера
Формованная сера бывает чешуйчатая и пластинчатая. Чешуйчатую серу начали производить на НПЗ в 1950-х годах. Для получения используют вращающийся барабан, внутри он охлаждается водой, а снаружи кристаллизуется сера в виде чешуек толщиной 0,5-0,7 мм.
В начале 1980-х вместо чешуйчатой стали выпускать пластинчатую серу. На движущуюся ленту подается расплав серы, который охлаждается по мере движения ленты. На выходе образуется застывший лист серы, который ломают с образованием пластинок.
Сегодня эта технология считается устаревшей, хотя около 40 % канадской серы экспортируется именно в таком виде ввиду больших капиталовложений в установки для ее получения.
Гранулированная сера
Гранулированную серу получают различными методами.
Водная грануляция (пеллетирование) разработана в 1964 году английской фирмой «Эллиот». Процесс основан на быстром охлаждении капель серы, падающих в воду. Первое внедрение технологии — процесс «Салпел» в 1965 году. Крупнейший завод позже был построен в Саудовской Аравии в 1986 году. На нем каждая из трех установок может производить до 3500 т гранулированной серы в сутки. Недостаток технологии - ограниченное качество гранул серы, обладающих неправильной формой и повышенной хрупкостью.
Грануляция в кипящем слое разработана французской компанией «Перломатик». Капли жидкой серы подаются вверх. Они охлаждаются водой и воздухом и смачиваются жидкой серой, которая застывает на образующихся гранулах тонким слоем. Конечный размер гранул 4-7 мм. Более прогрессивным является процесс «Прокор», который широко внедрен в Канаде. В нем применяются барабанные грануляторы. Однако этот процесс очень сложен в управлении.
Воздушно-башенная грануляция разработана и внедрена в Финляндии в 1962 году. Расплав серы диспергируется с помощью сжатого воздуха в верхней части грануляционной башни. Капли падают и затвердевают, попадая на транспортную ленту.
Молотая сера
Молотая сера является продуктом размола комовой серы. Степень измельчения может быть различной. Его проводят сначала в дробилке, потом в мельнице. Таким способом возможно получение очень высокодисперсной серы с размером частиц менее 2 мкм. Грануляцию порошковой серы проводят в прессах. Необходимо использование связующих добавок, в качестве которых используют битумы, стеариновую кислоту, жирные кислоты в виде водной эмульсии с триэтаноламином и другие.
Коллоидная сера
Коллоидная сера - это разновидность молотой серы с размером частиц менее 20 мкм. Ее применяют в сельском хозяйстве для борьбы с вредителями и в медицине как противовоспалительные и дезинфицирующие средства. Коллоидную серу получают различными способами.
Способ получения путем размола широко распространен, поскольку не предъявляет высоких требований к сырью. Одним из лидеров по этой технологии является фирма «Байер».
Способ получения из расплавленной серы или ее паров был внедрен в США в 1925 году. Технология подразумевает смешение с бентонитом, полученная смесь образует устойчивые суспензии с водой. Однако содержание серы в растворе невелико (не более 25 %).
Экстракционные способы получения основаны на растворении серы в органических растворителях и дальнейшем испарении последних. Однако они не получили широкого распространения.
Высокочистая сера
Высокочистую серу получают используя химические, дистилляционные и кристаллизационные методы. Ее применяют в электронной технике, при изготовлении оптических приборов, люминофоров, в производстве фармацевтических и косметических препаратов - лосьонов, мазей, средств против кожных болезней.
Применение серы
Об одном из самых древних (хотя и гипотетических!) применений серы рассказывают многие старинные книги. Как источник тепла при термообработке грешников серу живописуют и Новый и Ветхий заветы. И если книги такого рода не дают достаточных оснований для археологических раскопок в поисках остатков райских кущ или геенны огненной, то их свидетельство о том, что древние были знакомы с серой и некоторыми ее свойствами, можно принять на веру.
Одна из причин этой известности - распространенность самородной серы в странах древнейших цивилизаций. Месторождения этого желтого горючего вещества разрабатывались греками и римлянами, особенно в Сицилии, которая вплоть до конца прошлого века славилась в основном серой.
С древнейших времен серу использовали для религиозно-мистических целей, ее зажигали при различных церемониях и ритуалах.
Но так же давно элемент №16 приобрел и вполне мирские назначения: серой чернили оружие, ее употребляли при изготовлении косметических и лекарственных мазей, ее жгли для отбелки тканей и для борьбы с насекомыми. Добыча серы значительно увеличилась после того, как был изобретен черный порох. Ведь сера (вместе с углем и селитрой) - непременный его компонент.
Сера применяется:
- в первую очередь для получения серной кислоты;
- в бумажной промышленности для получения сульфитцеллюлозы;
- в сельском хозяйстве для борьбы с болезнями растений, главным образом винограда и хлопчатника;
- в резиновой промышленности вулканизующий агент;
- в производстве красителей и светящихся составов;
- для получения черного охотничьего пороха;
- в производстве спичек.
Сера в производстве серной кислоты
Основной потребитель серы - химическая промышленность. Примерно половина добываемой в мире серы идет на производство серной кислоты. Чтобы получить 1 т H2SО4, нужно сжечь около 300 кг серы. А роль серной кислоты в химической промышленности сравнима с ролью хлеба в нашем питании.
Сера в производстве спичек
Значительное количество серы (и серной кислоты) расходуется при производстве спичек.
Некое подобие спичек было изобретено в средневековом Китае. Это были тонкие щепочки с кончиками, пропитанными обыкновенной чистой серой. Зажигались они не путём чиркания, а путём соприкосновения с тлеющим трутом, и служили для облегчения процесса разжигания огня с помощью трута и огнива. Эти "прото-спички" упоминаются в китайских текстах XIII-XIV веков. К XV веку эта новинка дошла до Европы, но повсеместного распространения не получила. Подобные серные палочки стали использоваться в Европе только к XVII-XVIII векам, до тех пор, пока развитие химии не позволило их усовершенствовать.
Сера в производстве смазочных веществ
Соединения серы находят применение в нефтехимической промышленности. В частности, они необходимы при производстве антидетонаторов, смазочных веществ для аппаратуры сверхвысоких давлений; в охлаждающих маслах, ускоряющих обработку металла, содержится иногда до 18% серы.
Сера в производстве взрывчатых веществ
Элементарная сера и серная кислота в значительных количествах используются в производстве взрывчатых веществ. Особенно жесткие требования к сере предъявляются в производстве пороха она должна быть, например, освобождена от малейших примесей кремнезема.
Сера применяется в качестве исходного материала обычно только в производстве черного пороха и минного пороха на натровой селитре. В Соединенных Штатах Северной Америки серу применяют также в некоторых дешевых сортах бризантных взрывчатых веществ для горной промышленности.
Сера в производстве целлюлозы
Бумажная промышленность - это еще одна область, куда уходит значительная часть добытого вещества.
Соединения серы помогают выделить целлюлозу. Для того чтобы произвести 1 т целлюлозы, нужно затратить более 100 кг серы.
Сера в вулканизации каучуков
Много элементарной серы потребляет и резиновая промышленность - для вулканизации каучуков.
Для вулканизации применяют природную молотую серу. Элементная сера имеет несколько кристаллических модификаций, из которых только a-модификация частично растворима в каучуке. Именно эта модификация, имеющая температуру плавления 112,7 ºС, и используется при вулканизации.
Сера в строительстве
Использование серы в строительстве в виде серных мастик и растворов было известно еще в XIX в. В 1859г. А. X. РАЙТ получил патент на применение серных растворов для заливки фундаментных болтов. Серные мастики и растворы использовались в прошлом веке и в Российской Федерации для заливки швов каменных кладок и особенно эффективно для заделки металлических стоек перил лестничных маршей и металлических связей каменных конструкций взамен расплавленного свинца.
В дальнейшем, с развитием антикоррозионной службы, серные мастики и растворы, получившие название серных цементов, применяли для заливки швов при футеровке различных емкостей, аппаратов и строительных конструкций штучными кислотоупорными материалами, эксплуатируемых в условиях агрессивного воздействия.
Сера в сельском хозяйстве
В сельском хозяйстве сера применяется как в элементарном виде, так и в различных соединениях. Она входит в состав минеральных удобрений и препаратов для борьбы с вредителями. Наряду с фосфором, калием и другими элементами сера необходима растениям.
Впрочем, большая часть вносимой в почву серы не усваивается ими, но помогает усваивать фосфор. Серу вводят в почву вместе с фосфоритной мукой.
Имеющиеся в почве бактерии окисляют ее, образующиеся серная и сернистая кислоты реагируют с фосфоритами, и в результате получаются фосфорные соединения, хорошо усваиваемые растениями.
Сера в медицине и фармацевтике
В медицинской практике применение серы основано на ее способности при взаимодействии с органических веществами организма образовывать сульфиды и пентатионовую кислоту, от присутствия которых зависят кератолитические (растворяющие - от греч. keras - рог и lytikos -растворяющий), противомикробные и противопаразитарные эффекты.
Все сульфамидные препараты - сульфидин, сульфазол, норсульфазол, сульгин, сульфодимезин, стрептоцид и другие подавляют активность многочисленных микробов. И все эти лекарства - органические соединения серы.
После появления антибиотиков роль сульфамидных препаратов несколько уменьшилась. Впрочем, и многие антибиотики можно рассматривать как органические производные серы. В частности, она обязательно входит в состав пенициллина.
Мелкодисперсная элементарная сера - основа мазей, применяемых при лечении грибковых заболеваний кожи.
Сера входит в состав мази Вилькинсона и других препаратов, применяемых для лечения чесотки. Очищенную и осажденную Серу употребляют в мазях и присыпках для лечения некоторых кожных заболеваний (себорея, псориаз и других); в порошке - при глистных инвазиях (энтеробиоз); в растворах - для пиротерапии прогрессивного паралича и других.
Сера в косметике
Серу называют минералом красоты за ее способность улучшать состояние кожи, волос, зубов, ногтей. Наиболее полно способность МСМ омолаживать и восстанавливать кожу проявляется при непосредственном нанесении на кожу. Применяется для снижения остроты и профилактики аллергических реакций, для профилактики синдрома хронической усталости, псориаза, в программах снижения веса и для борьбы с угревой сыпью.
Вред серы для окружающей среды
По своему отрицательному воздействию на окружающую среду и человека сера (точнее, ее соединения) стоит на одном из первых мест. Основной источник загрязнения серой - сжигание каменного угля и других видов топлива, содержащих серу. При этом около 96% серы, содержащейся в топливе, попадает в атмосферу в виде сернистого газа SO2.
Химическое отравление природы
В атмосфере сернистый газ постепенно окисляется до оксида серы (VI). Оба оксида - и оксид серы (IV), и оксид серы (VI) - взаимодействуют с парами воды с образованием кислотного раствора. Затем эти растворы выпадают в виде кислотных дождей.
Оказавшись в почве, кислотные воды угнетают развитие почвенной фауны и растений. В результате создаются неблагоприятные условия для развития растительности, особенно в северных регионах, где к суровому климату добавляется химическое загрязнение. В результате гибнут леса, нарушается травяной покров, ухудшается состояние водоемов.
Кислотные дожди разрушают изготовленные из мрамора и других материалов памятники, более того, они вызывают разрушение даже каменных зданий и изделий из металлов. Поэтому приходится принимать разнообразные меры по предотвращению попадания соединений серы из топлива в атмосферу. Для этого подвергают очистке от соединений серы нефть и нефтепродукты, очищают образующиеся при сжигании топлива газы.
Сама по себе сера в виде пыли раздражает слизистые оболочки, органы дыхания и может вызывать серьезные заболевания. ПДК серы в воздухе 0,07 мг/м3.
Многие соединения серы токсичны. Особенно следует отметить сероводород, вдыхание которого быстро вызывает притупление реакции на его неприятный запах и может привести к тяжелым отравлениям даже с летальным исходом. ПДК сероводорода в воздухе рабочих помещений 10 мг/м3, в атмосферном воздухе 0,008 мг/м3.
Пожароопасность серы
Тонкоизмельченная сера склонна к химическому самовозгоранию в присутствии влаги, при контакте с окислителями, а также в смеси с углём, жирами, маслами. Сера образует взрывчатые смеси с нитратами, хлоратами и перхлоратами. Самовозгорается при контакте с хлорной известью.
Средства тушения: распылённая вода, воздушно-механическая пена.
По данным В. Маршалла пыль серы относится к разряду взрывоопасных, но для взрыва необходима достаточно высокая концентрация пыли - порядка 20 г/м³ (20 000 мг/м³), такая концентрация во много раз превышает предельно допустимую концентрацию для человека в воздухе рабочей зоны - 6 мг/м³.
Пары образуют с воздухом взрывчатую смесь.
Горение серы протекает только в расплавленном состоянии аналогично горению жидкостей. Верхний слой горящей серы кипит, создавая пары, которые образуют слабосветящееся пламя высотой до 5 см. Температура пламени при горении серы составляет 1820 °C.
Так как воздух по объёму состоит приблизительно из 21 % кислорода и 79 % азота и при горении серы из одного объёма кислорода получается один объём SO2, то максимальное теоретически возможное содержание SO2 в газовой смеси составляет 21 %. На практике горение происходит с некоторым избытком воздуха, и объёмное содержание SO2 в газовой смеси меньше теоретически возможного, составляя обычно 14…15 %.
Обнаружение горения серы пожарной автоматикой является трудной проблемой. Пламя сложно обнаружить человеческим глазом или видеокамерой, спектр голубого пламени лежит в основном в ультрафиолетовом диапазоне. Тепловыделение при пожаре приводит к температуре ниже, чем при пожарах других распространенных пожароопасных веществ.
Для обнаружения горения тепловым извещателем необходимо размещать его непосредственно близко к сере. Пламя серы не излучает в инфракрасном диапазоне. Таким образом оно не будет обнаружено распространёнными инфракрасными извещателями. Ими будут обнаруживаться лишь вторичные возгорания. Пламя серы не выделяет паров воды. Таким образом детекторы ультрафиолетовых извещателей пламени, использующие соединения никеля, не будут работать.
Для эффективного обнаружения пламени рекомендуется использовать ультрафиолетовые извещатели с детекторами на основе молибдена. Они имеют спектральный диапазон чувствительности 1850…2650 ангстрем, который подходит для обнаружения горения серы.
Для выполнения требований пожарной безопасности на складах серы необходимо:
- конструкции и технологическое оборудование должны регулярно очищаться от пыли;
- помещение склада должно постоянно проветриваться естественной вентиляцией при открытых дверях;
- дробление комков серы на решётке бункера должно производиться деревянными кувалдами или инструментом из неискрящего материала;
- конвейеры для подачи серы в производственные помещения должны быть снабжены металлоискателями;
- в местах хранения и применения серы необходимо предусматривать устройства (бортики, пороги с пандусом и т. п.), обеспечивающие в аварийной ситуации предотвращение растекания расплава серы за пределы помещения или открытой площадки.
На складе серы запрещается:
- производство всех видов работ с применением открытого огня;
- складировать и хранить промасленную ветошь и тряпки;
- при ремонте применять инструмент из искродающего материала.
Пожары на складах серы
В декабре 1995 года на открытом складе серы предприятия, расположенного в городе Сомерсет-Уэст Западной Капской провинции Южно-Африканской Республики, произошёл крупный пожар, погибли два человека.
16 января 2006 г. около пяти вечера на череповецком предприятии «Аммофос» загорелся склад с серой. Общая площадь пожара - около 250 квадратных метров. Полностью ликвидировать его удалось лишь в начале второго ночи. Жертв и пострадавших нет.
15 марта 2007 года рано утром на ООО «Балаковский завод волоконных материалов» произошёл пожар на закрытом складе серы. Площадь пожара составила 20 кв.м. На пожаре работало 4 пожарных расчёта с личным составом в 13 человек. Примерно через полчаса пожар был ликвидирован. Никто не пострадал.
4 и 9 марта 2008 года произошло возгорание серы в Атырауской области в хранилище серы ТШО на Тенгизском месторождении. В первом случае очаг возгорания удалось потушить быстро, во втором случае сера горела 4 часа. Объём горевших отходов нефтепереработки, к каковым по казахстанским законам отнесена сера, составил более 9 тысяч килограммов.
В апреле 2008 недалеко от посёлка Кряж Самарской области загорелся склад, на котором хранилось 70 тонн серы. Пожару была присвоена вторая категория сложности. К месту происшествия выехали 11 пожарных расчётов и спасатели. В тот момент, когда пожарные оказались около склада, горела ещё не вся сера, а только её небольшая часть - около 300 килограммов. Площадь возгорания вместе с участками сухой травы, прилегающими к складу, составила 80 квадратных метров. Пожарным удалось быстро сбить пламя и локализовать пожар: очаги возгорания были засыпаны землёй и залиты водой.
В июле 2009 в Днепродзержинске горела сера. Пожар произошёл на одном из коксохимических предприятий в Баглейском районе города. Огонь охватил более восьми тонн серы. Никто из сотрудников комбината не пострадал.
В конце июля 2012 под Уфой в поселке Тимашево загорелся склад с серой площадью 3200 квадратных метров. На место выехало 13 единиц техники, в тушении пожара задействован 31 пожарный. Произошло загрязнение атмосферного воздуха продуктами горения. Погибших и пострадавших нет.
Мировой рынок серы
Общемировые запасы элементарной серы составляют около 5 млрд. т. В целом, мировая серная Промышленность может быть разделена на два сектора по формам добычи серы: специализированный и «побочный».
Мировая добыча серы
Специализированный сектор ориентируется исключительно на добычу серы или пиритов из месторождений данного сырья. Данный сектор составляет около 10,5% от всего объема общемировой добычи серы.
Небольшие объемы чистой серы производятся в Азии, Европе и Южной Америке. Но стоит отметить, что значимость пиритов для глобального предложения серы значительно снизилась, так как только в Китае и Финляндии, в отличие от других стран-производителей серы, пириты обеспечивают ключевой объем добычи серы. Показательно, что около 80% мировой добычи пиритов приходится именно на Китай.
В «побочном» секторе, сера или серная кислота вырабатывается в качестве вынужденно побочного продукта в процессе переработки нефти, Природного газа, других ресурсов, причем уровень выработки серы зависит не от объемов потребления в мире, а от объемов очищаемого от нее сырья.
Из 25 стран, которые производят более 500 тыс. т серы в год, 18 получают подавляющую долю их производства серы в процессе ее косвенной выработки из другого сырья. Отметим, что на 25 ведущих стран приходится около 92,9% общемировой добычи серы.
Мировое производство серы
В 2011 году, по данным U. S. Geological Survey, производство серы в мире составило порядка 69 млн т. Около 63,8 % этого объема пришлось на элементарную серу, полученную главным образом при переработке нефти 49,8 % и Природного газа 44,3 %, а также при освоении месторождений самородной серы 1,2 %.
Еще 29 % на отходящие газы цветной металлургии, коксовые газы, кислый гудрон заводов по переработке нефти и другое сырье, используемое в основном для прямого выпуска серной кислоты. И только 7,2 % на пириты.
Крупнейшими производителями серы на глобальном рынке сегодня являются Китай 13,9 %, США 12,8 %, Канада 10,3 и Россия 10,3 %. На долю стран Ближнего Востока суммарно приходится 12,8 % мирового эмиссии ценных бумаг серы.
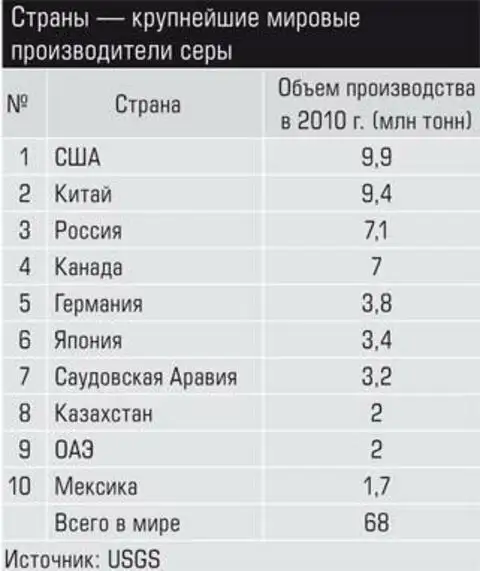
Крупнейшие мировые производители серы
Основные объемы газовой и нефтяной серы производят компании:
- ExxonMobil;
- ConocoPhillips;
- Valero Energy, один из крупнейших переработчиков нефти в США;
- британская BP;
- англо-голландская Shell;
- CITGO Petroleum дочерняя структура Petrоleos de Republic Venezuela;
- российский «Газпром».
В начале XXI века основными производителями серы в России являются предприятия ОАО Газпром: ООО Газпром добыча Астрахань и ООО Газпром добыча Оренбург, получающие её как побочный продукт при очистке газа.
Мировое потребление серы
Около 90 % всей получаемой в мире серы сегодня перерабатывается и затем потребляется в виде серной кислоты. Приблизительно 65 % серной кислоты используется для производства фосфорных и комплексных удобрений. Еще 11-12 % приходится на другие области сельского хозяйства, выработку сульфата аммония и прочих серосодержащих удобрений, средств защиты от вредителей и различных химикатов.
Остальное на горнодобывающую промышленность - выщелачивание медных и других руд, химический комплекс - производство синтетических каучуков и резинотехнических изделий, красителей, искусственных волокон и так далее, нефтяную отрасль - приготовление буровых растворов, алкилирование в нефтепереработке и целлюлозно-бумажную промышленность - сульфитная и сульфатная варка целлюлозы.
Основными импортерами серы сегодня являются Индия 6%, Южная Америка 7%, США 10%, Северная и Южная Африка 24%, и Китай 32%.
Мировой рынок серы не отличается стабильностью. Положительное влияние на конъюнктуру оказывает рост населения мира, климатические изменения и природные катаклизмы, сокращение сельхозугодий, увеличение спроса на продовольствие, стремительное развитие промышленности таких стран, как Китай, Индия и Бразилия.
В то же время ввод в эксплуатацию новых нефтегазовых месторождений с высоким содержанием серы в сырье, а также переход к более глубокой очистке. Ситуацию усугубляет и политика отдельных стран, крупнейших потребителей серы.
Например, Китай, как и в случае с импортом нефти, старается закупать сырье по минимальной стоимости, которая зачастую оказывается невыгодной производителю. А в качестве меры убеждения уходит с рынка, что приводит к его затовариванию и обвалу цен.
Регулировать объемы добычи серы в соответствии с колебаниями рынка не представляется возможным, это обусловлено тем, что подавляющая ее часть получается попутно при производстве других целевых продуктов.
В результате с 2000 года мировой выпуск серы превышал ее потребление, кроме периода 2004-2006 годов, когда спрос резко вырос благодаря введению новых мощностей по выпуску фосфатных удобрений и развитию металлургической промышленности в США, Южной Америке, Африке и Восточной Азии. В Канаде, Казахстане и России были накоплены значительные объемы нереализованной серы.
Мировые цены на серу
Поэтому цены на серу были достаточно низкими, за исключением 2008 года, когда они выросли более чем в 10 раз и достигли 800 долларов за тонну. К настоящему времени, после резкого падения в период глобального финансовоэкономического кризиса, они вернулись к своим средним показателям в 150-200 долларов.
На текущий момент мировой рынок серы относительно сбалансирован. Как в прошлом, так и в нынешнем году конъюнктура способствует размещению серы по ценам, которые позволяют получать прибыль.
Но перспективы развития рынка связаны прежде всего с планируемым широкомасштабным вводом на Ближнем Востоке новых мощностей по добыче и переработке углеводородов в 2014-2015 годах. Очевидно, что последствием этого станет резкий рост конкуренции на глобальном рынке между производителями серы.
Авторы, источники и ссылки
Создатель статьи
Автором данной статьи является Панкратова Татьяна Владимировна
vk.com/panyt2008 - профиль автора Вконтакте
Facebook.com/profile.php?id=1849770813 - профиль автора статьи в Facebook
odnoklassniki.ru/profile513850852201- профиль автора данной статьи в Однокласниках
plus.Google.com/114249854655731943816 - профиль автора материала в Гугл+
my.mail.ru/mail/pany-t2008 - профиль автора данного материала в Мой мир
Твиттер.com/Kollega7- профиль создателя статьи в Твитере
layma-1000.livejournal.com - блог создателя данной статьи в Живом Журнале
Ответственные администраторы
Корректировщик статьи - Джейкоб
Рецензент статьи - профессор, д. э. н. Хайзенберг
Главный редактор ForexAW.com - Варис смотрящий
Источники текстов
wikipedia.org - свободная электронная энциклопедия Википедия
ru.wiktionary.org - электронный информационный онлайн Викисловарь
dic.academic.ru - словари и энциклопедии на портале Академик
bibliotekar.ru - электронная онлайн-библиотека Библиотекарь
studopedia.org - онлайн-энциклопедия для студентов Студопедия
wikiznanie.ru -электронная онлайн-энциклопедия Викизнание
bibliofond.ru - электронная онлайн-библиотека Библиофонд
grandars.ru - электронная экономическая энциклопедия Грандарс
dictionary-economics.ru - онлайн-словарь экономических терминов
studme.org - сайт с учебными материалами для студентов
abc.informbureau.com - онлайн-словарь экономических терминов
tolkslovar.ru - онлайн-сборник толковых словарей
chto-eto-takoe.ru - энциклопедический сайт о значениях слов
aif.ru - электронная газета Аргументы и факты
classes.ru - электронный сборник онлайн-словарей
slovarslov.ru - сборник словарей русского языка
ria.ru - сайт информационного агентства РИА
onlinedics.ru - крупнейший сборник онлайн-словарей
slovariya.ru - словари по экономике и юриспруденции
files.school-collection.edu.ru - сайт с материалами для учащихся
chem100.ru - электронный онлайн-справочник химика
xumuk.ru - информационный сайт о химии
webeconomy.ru - информационный сайт о всемирной экономике
ngpedia.ru - онлайн-энциклопедия нефти и газа
djht.ru - сайт с информацией по химии
chem21.info - сайт о химии и химической технологии
mirznanii.com - сайт для студентов Мир знаний
mining-enc.ru - электронная Горная энциклопедия
tvoi-uvelirr.ru - портал об искусстве Твой ювелир
subref.ru - сайт с учебными работами для студентов
kazenergy.com - сайт Казахстанской ассоциации организаций нефтегазового и энергетического комплекса «KAZENERGY»
n-t.ru - электронная библиотека Наука и техника
webelements.narod.ru - сайт о периодической системе Менделеева
mineral-gum.com - официальный сайт компании MineralGum
helpiks.org - сайт с полезными советами Хелпикс
vseslova.com.ua - сборник электронных словарей русского языка
newslab.ru - электронная онлайн-газета Ньюслаб Ру
termin.bposd.ru - словарь терминов, понятий и определений
poiskslov.com - сборник словарей русского языка
znachenieslova.ru - электронный сборник онайн-словарей
bionow.ru - сайт о современной биологии
psylist.net - информационный сайт о психологии
zhivotnovodstvo.net.ru - информационный сайт о животноводстве
medbiol.ru - сайт о медицине и биологии
polnaja-jenciklopedija.ru - справочник для учащихся Полная энциклопедия
bigreferat.ru - сайт с учебными материалами для студентов
forum.aroma-vita.com.ua - форум о косметических средствах
betony.ru - сайт о строительных материалах
newchemistry.ru - информационный сайт о химии
Использованные сервисы
forexaw.com - информационно-аналитический портал по финансовым рынкам
Google.ru - крупнейшая поисковая система в мире
youtube.com - видеохостинг с видео различной тематики
rutube.ru - видеохостинг с различным видео
video.google.com - поиск видео в интернете черег Google Inc.
translate.google.ru - переводчик от поисковой системы Google Inc.
maps.google.ru - карты от Google Inc. для поиска мест описываемых в материале
Yandex.ru - крупнейшая поисковая система в России
wordstat.yandex.ru - сервис от Яндекса позволяющий анализировать поисковые запросы
video.yandex.ru - поиск видео в интернете через Яндекс
images.yandex.ru - поиск картинок через сервис Яндекса
maps.yandex.ru- карты от Яндекса для поиска мест описываемых в материале
finance.yahoo.com - данные о финансовом состоянии компаний
Google.com/finance - финансовый сервис системы Google Inc.
otvet.mail.ru - сервис ответов на вопросы
rabota.mail.ru - сервис поиска работы, вакансий и информации о компаниях
slovari.yandex.ua - сервис словарей на Яндексе
help.yandex.ru - сервис компьютерной помощи на Яндексе